原标题:诺华依维莫司招募30名中国胰腺神经内分泌瘤患者

药物介绍 “依维莫司(everolimus ,RAD001片)”是知名药企诺华(Novartis)开发的口服mTOR抑制剂。全球范围内,该药已获批可用于:实体器官移植免疫抑制治疗排斥反应(对应商品名:美国的“Zortress”,或欧州的“Certican”),及肿瘤适应症(对应商品名:美国的“Afinitor/飞尼妥”,或欧洲的“Votubia”)。本次非随机化、多中心、4期临床的招募对象为,局部晚期或转移性、分化良好的进行性胰神经内分泌瘤(pNET)患者,主要评估这些患者使用依维莫司的有效性和安全性。目前临床招募范围面向中国患者,国内有6家医院参与。计划入组人数30人。
本期临床招募和实施方案,已经在中国国家食品药品监督管理总局登记注册(注册号:CTR20160035)。按照本次临床实施方案规定,入选患者将接受“依维莫司”方案治疗。
本期临床招募的入选条件包括:
1年龄≥18岁的中国成人患者
2患者必须已经被组织学检查确认为G1或G2期胰神经内分泌瘤(pNET)(WHO 2010)
3患者在入组之前的12个月内必须有证明疾病进展的放射学证据(按RECIST 1.1评价)
4通过增强CT或者MRI进行放射学评估,根据RECIST 1.1标准评价为可测量疾病。
5治疗医师建议给予RAD001治疗
详细的入选和排除标准,请访问文末网址链接。符合所有合格性条件的患者,在参与本次临床实施方案过程中,将可获得免费的研究相关检查和治疗。您如有兴趣参与,请和以下研究人员和临床参加机构(医院)取得联系:
主要研究者信息:
负责人:徐建明 教授
电子邮箱: jmxu2003@163.com
单位名称:解放军307医院
(其他主要研究者见下表)
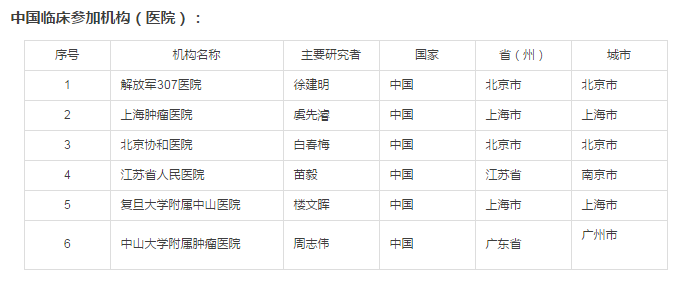
来源: e药环球

